 8
8
我公司专业办理医疗产品出口欧盟、美国、中东南美等国家的各种认证:
TUV莱茵,TUV南德,***等CE认证,全套CE技术文件编订, CE*四版临床评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:2016,医疗器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请), FDA QSR820验厂辅导及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系辅导/OTC验厂辅导及整改,英国BRC认证咨询,BSCI验厂辅导;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令辅导)
1.法规背景
2016年6月,欧盟会(European Commission)发布了*四版医疗器械临床评价的指导原则(MEDDEV 2.7.1 Rev.4)。和2009年*三版的指导原则相比,直观的变化就是文件的页数从46页变为了65页,更新的版本不仅包含了新的要求,还有对以前要求的进一步细化,扩展和澄清,同时还有一些举例以帮助生产商实施临床评价。
MEDDEV2.7/1从性质上来说是一份指导原则,所以它没有所谓的“生效日期”,由每一个公告机构自行决定*三版的失效日期及*四版的实施日期。目前大多数的公告机构如TUV南德(NB 0123)已经不再接受基于*三版指导原则的临床评价报告;之前按照*三版完成临床评价获得CE证书的产品也会在监督审核的时候被要求按照*四版进行补充评价即更新撰写。
此外,该指导原则的发布时间碰巧在2016年6月15日MDR(草稿)文本发布之后,所以指导原则的要求也与新法规的临床评价的要求较为接近。所以该指导原则也可以作为向新法规过渡的一个工具。
2. MEDDEV 2.7.1 Rev4主要变化
2.1主要变化之一:临床报告更新的频率
按照新版临床报告指南的要求,对于高风险或者新设备,应每年更新;对于低风险的设备,每2‐5年更新。对于如何确定更新的额频率需要有定义。对于任何风险类别的器械,如果从PMS收集到的信息影响到评价或者结论,CER需要进行更新。
2.2主要变化之二:报告编写人和评价人的
按照新版临床报告指南的要求,对于临床报告的编写人提出了要求。包括需要有相关专业的高等教育学位以及至少五年的专业经历,或者十年的专业工作经历,如果学位不够的话。如果不能满足要求,需要对其进行判定和说明。
2.3 主要变化之三:评价报告需要有明确的可测量的目标
*四版临床评估指南对于临床评估报告的目的有更明确的描述,需要与器械的安全性、性能以及风险‐收益平衡进行更加清晰和详细的描述,在指南的*7部分和附件5中有详细的描述。
2.4主要变化之四:确定技术发展水平
*四版临床评估指南对于设备的技术发展水平和处理方式的建立和文件化,提供了更加详细的描述。这包括确定设备的安全性和性能,以及被宣称的比对器械,行业的基准器械,或者其他的类似器械;需要包括风险和收益的分析。
2.5 主要变化之五:数据的科学性和有效性
*四版临床评估指南非常强调数据的科学性和有效性,包括从统计学考虑。这贯穿于整个指南文件规定的阶段,包括影响数据完整性的因素,数据的客观性和权重,文件搜集的方法,数据的评估和权重,数据是否阐述了符合性的分析。
2.6 主要变化之六:比对器械
*四版临床评估指南对于评估器械和比对器械的等效有了更加详细的规定,特别强调对于比对器械的数据的可获得性。需要从临床数据、技术参数、生物性能三个方面逐一比对,确保所有比对的内容不存在差异。
2.7 主要变化之七:比对器械的数据获得
*四版临床评估指南要求公告机构对于企业是否能够获得比对器械的数据进行挑战,这个被认为是法规的一个转折点,这要求制造商需要有一个被允许接触竞争对手的器械数据的协议。
2.8 主要变化之八:什么时候需要临床试验
*四版临床评估指南附件2详细描述了器械的风险以及制造商怎么决定是否具备了充分的临床证据。
2.9 主要变化之九:风险‐收益
附件7提供了详细的指南,对于器械的安全性和性能表述;
附件7.2讨论了风险和收益分析,包括对于风险和收益的量的评估,以及总体评价。交付后的数据价值,以及可能会影响统计有效性行的因素等。
2.10 主要变化之十:售后监督和售后临床跟踪
我公司专业办理医疗产品出口欧盟、美国、中东南美等国家的各种认证:
TUV莱茵,TUV南德,***等CE认证,全套CE技术文件编订, CE*四版临床评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:二016,医疗器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请), FDA QSR820验厂辅导及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系辅导/OTC验厂辅导及整改,英国BRC认证咨询,BSCI验厂辅导;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令辅导)。
ce*四版临床评价报告
CE*四版临床评价,随着MEDDEV 2.7.1*四版的且没有新旧版本的过渡期,符合制造商大利益的做法便是从现在开始与公告机构讨论如何开始实施这些新要求并从现在开始执行差距评估和资源需求评估。CE*四版临床评价,差距评估已迫在眉睫,因为制造商需要尽快为额外的临床数据进行预算。因此,如果临床试验需要在2019年启动的话,则需要将评估成本记入明年的预算计划内。
CE*四版临床评价,关于MEDDEV2.7.1 Rev 4,我司可以协助您:
1、协助建立临床评价程序;
2、建立临床评价方案
3、寻找等同产品,进行等同分析;
4、搜索文献及其他临床数据;
5、临床数据分析;
6、完成临床评价报告。
CE*四版临床评价,我司可办CE技术文件的整改,CE技术文件的编订,风险管理报告的编写,依据MEDDEV2.7.1Rev4编写的临床评估报告,欧盟代表服务,自由销售certificateCFS,美国FDA注册,FDA验厂辅导等。CE*四版临床评价,报告编写人和评价人的 按照新版临床报告指南的要求,对于临床报告的编写人提出了要求。包括需要有相关专业的高等教育学位以及至少五年的专业经历,或者十年的专业工作经历,如果学位不够的话。如果不能满足要求,需要对其进行判定和说明。
CE*四版临床评价,临床报告更新的频率 按照新版临床报告指南的要求,对于高风险或者新设备,应每年更新;对于低风险的设备,每2-5年更新。CE*四版临床评价,对于如何确定更新的额频率需要有定义。对于任何风险类别的器械,如果从PMS收集到的信息影响到评价或者结论,CER需要进行更新。
MDR&IVDR法规的变化(2)
2. 新增和细化医疗器械分类
- 22个分类规则,增加了4个规则。
新增software分类
新增用于灭菌的器械
新增利用无活性的人类组织或细胞,
或其物制造的器械
新增由纳米材料合成或制成的器械
部分以美容为目的的产品纳入医疗
器械进行管理
3 .变更CE符合评估途径
Annex IX Conformity assessment based on
a QMS and assessment of the T.D.
Annex X Conformity based on type examination
Annex XI Conformity based on product conformity verification
MDR范围的变化
MDR纳入更多产品进行管理;
• MDR中附录XIV所列的非医疗用途的产品:
• 隐形眼镜;
• 用于修改或固定身体部位的植入物;
• 面部或其他皮肤或粘膜填充剂;
• 吸脂设备;
• 用于人体的有创激光设备;
• 强脉冲光设备
我公司专业办理医疗产品出口欧盟、美国、中东南美等国家的各种认证:
TUV莱茵,TUV南德,***等CE认证,全套CE技术文件编订, CE*四版临床评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:2016,医疗器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请), FDA QSR820验厂辅导及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系辅导/OTC验厂辅导及整改,英国BRC认证咨询,BSCI验厂辅导;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令辅导)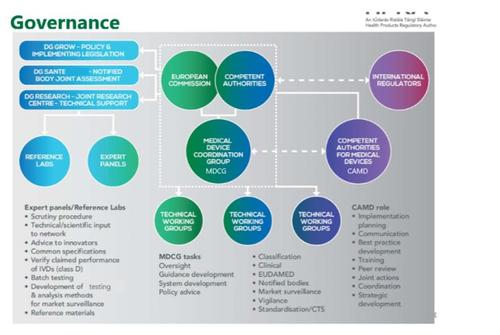
我公司专业办理医疗产品出口欧盟、美国、中东南美等国家的各种认证:
TUV莱茵,TUV南德,***等CE认证,全套CE技术文件编订, CE*四版临床评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:2016,医疗器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请), FDA QSR820验厂辅导及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系辅导/OTC验厂辅导及整改,英国BRC认证咨询,BSCI验厂辅导;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令辅导)。
阶段0:确定临床评估的范围及计划
临床评估开始之前,制造商应根据基本要求,需要从临床角度及器械历史及性质定义评估的范围及计划。
阶段1:相关数据的识别
用于临床评估的数据总的来说主要来自两个方面:制造商生成和持有的数据以及文献中的数据。其中,制造商生成和持有的数据包括:
(1)所有的上市前的临床研究;
(2)制造商在欧洲或其他国家进行的风险管理活动以及PMS项目;
(3)相关的临床前研究。
阶段2:相关数据的评估
为了确定阶段1获得的数据是否有价值,评估者应评估每一份文件对其临床性能和临床安全性的贡献。为了确保系统公正的评价数据,评估者在评估之前应当建立一个评估计划,用于确定评估过程和标准。
阶段3:临床数据分析
数据分析阶段的主要目标是确定当器械按其预期目的使用时,评估可供医疗器械使用的的数据集是否能证明符合器械临床性能和临床安全的基本要求。为证明符合性,评估者应从以下几个方面考虑:
(1)使用合理的方法;
(2)综合分析;
(3)考虑是否有增加临床研究及其他措施的必要;
(4)确定PMCF的需求。
阶段4:撰写临床评价报告 (可提供代理编写或更新:TUV南德/TUV莱茵/***/BSI/KIWA等公告机构要求的欧盟*四版医疗器械临床评价/评估报告、CE整套技术文件编订服务。)
对于所有的评价结果,将以报告的形式输出,即为临床评价报告。临床评价报告总结并汇总了所有相关的临床数据,并在技术文档的其他部分进行了记录或参考。
5、谁应该实施临床评价
临床评价应由合适的个人或团队进行。
制造商定义评价者的需求;
a)制造商应能够通过参考他们的资格和经验,来证明对评估者的选择,并为每一个评价者提出一个利益声明。
b)作为一般原则,评价者应具备以下知识:
●研究方法学(包括临床试验设计和生物统计学)
●信息管理(例如学科背景或图书馆员资格;相关数据库经验)
●法规需求
●医学写作(如有关科学或医学方面的研究生经验;有医学写作、系统复习和临床数据评估方面的培训和经验。
c)对于评估中的特定设备,评估者应该添加以下知识:
●器械的技术和应用
●诊断和管理的条件拟被设备、医疗替代品的知识、**标准和技术诊断或管理(例如相关医学专业的临床*)
d)评价者应该在相关领域具有以下培训和经验:
●在相关领域接受高等教育的学位和5年的专业经验;或
●如果没有相关学位,需要10年的专业经验。
我公司专业办理医疗产品出口欧盟、美国、中东南美等国家的各种认证:
TUV莱茵,TUV南德,***等CE认证,全套CE技术文件编订, CE*四版临床评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:2016,医疗器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请), FDA QSR820验厂辅导及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系辅导/OTC验厂辅导及整改,英国BRC认证咨询,BSCI验厂辅导;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令辅导)
NB应满足的要求-Annex VII
• MDR对NB的要求更加严格
• NB的授权和监管由多个国家主管当局联合组成的审核小组进行审核;
• NB必须要有自己的审核*团队,新法规下对外聘*的做法将有所限制;
• NB必须要有自己的临床*,而不能仅靠外部临床*进行相关审核。
• 新法规生效后, NB将按照新的要求重新授权,不符合要求的NB将会被淘汰。
• 对于已经取得CE证的企业,应密切关注其NB的新授权以及授权范围!!
MDR&IVDR修订要点
1) 强化符合性评审程序, 临床试验和临床评估, 警戒系统和市场监督系统, 确保医疗
器械的透明和可追溯性
2) MDD + AIMD →MDR; IVDD →IVDR
3) 药品, 化妆品和食品不在MDR/IVDR的范围内
4) MDR包括含有无活性的人组织或细胞的医疗器械
5) 无医疗用途, 但功能和风险与医疗器械类似的产品也纳入MDR
6) 含纳米材料的医疗器械要进严格的评估
定义: Commission Recommendation 2011/696/EU (OJ L 275, 20.10.2011, p.
38).
7) 电子商务服务 Information Society Service要符合Directive (EU) 2015/1535
8) 通用规范CS (Common Specification)
9) 规定经销链相关方 (Economic Operator) 的职责
10) MDD/AIMD中的Annex 的临床评估 或警戒系统纳入到了MDR的正文里
11) 医疗机构内部使用的器械
12) 缺陷产品对患者的补偿
13) 风险管理和临床评估互相依赖, 定期更新
14) 法规负责人需要满足要求, 负责监督和和控制医疗器械的生产, PMS和警戒
系统的活动. ---- 类似于质量授权人
15) 欧盟代表与进口商和制造商一起起到连带责任
欧盟代表要求, 类似于法规负责人
16) 平行贸 Parallel Trade, 特别是重新贴标签或重新包装
17) 一次性医疗器械的再加工和使用:
- 符合成员国的法规要求
- 再加工方要承担法定制造商的责任;
- 由医疗机构或外部加工方进行的一次性MD的再加工和再使用必须要符合通用
技术规范或协调标准或成员国的法规要求.
- 再加工器械的安全和性能应等同于初期的一次性MD
18) 植入器械: 患者应获得基本的信息, 包括标识, 危害健康的警示或注意事项
19) 带有CE标记的MD, 在欧盟内可以自由流通和销售. 但成员国可以限制某些器械
的使用.
20) 除了定制器械外, 所有器械都应应用UDI系统 (MDR执行后1-5年)
21) EUDAMed, MD的 命名Code
22) 植入和III类产品的制造商应公开产品的主要安全和性能, 及临床评估结果的概要.
- 安全和性能的概要应特别包括该产品在与其他诊断或**方法比较时的重要性,和二者的特殊使用条件
23) 在欧盟的层面上管理NB
24) 主管当局严格监控NB对技术文档, 特别是临床评估的评审
25) NB的飞行检查, 并对产品进行外观或实验室测试
26) 对输入或导出药物的III类植入产品和IIb有源产品, 欧盟*的*组应复审企业的临床评估报告, 并通告主管当局
27) III类产品和某些IIb产品, 制造商在临床评估或临床试验之前, 可以自愿地与*组联系, 咨询临床开发策略和临床试验方案.
28) 符合性评估时的产品分类: 按照国际实践分为四大类; 有源植入器械分为
---- (59)
29) Class III custom-made implantable devices 需要CE认证
30) 明确CE技术文件要求(Annex II & III)
我公司专业办理医疗产品出口欧盟、美国、中东南美等国家的各种认证:
TUV莱茵,TUV南德,***等CE认证,全套CE技术文件编订, CE*四版临床评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:2016,医疗器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请), FDA QSR820验厂辅导及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系辅导/OTC验厂辅导及整改,英国BRC认证咨询,BSCI验厂辅导;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令辅导)。