 8
8
口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令辅导)。
EN14683:欧盟医用口罩标准
VFE:过滤效率
PFE:颗粒过滤效率
ASTM F2100:美国医用口罩标准
欧盟标准 EN 14683
有三种测试方法用来给医用口罩进行分类:
1. 体外过滤率(BFE)(ASTM F2101-07)
• 这个测试是用来确定外科口罩上残留的源,此源直接影响到手术室空气中由口罩中释放出的数目。
• 测试方法:使用一个喷雾装置,用来释放出固定流量的空气流,这个空气流包含着一定浓度的金葡萄球菌,让这股空气流穿过包含所有层的外科口罩。喷雾口的平均尺寸为3微米。通过样品的数目和没有样品时的数目进行比较。
• 这个BFE比值越高,说明口罩能更好的保护病人不易因为手术人员而感染。
• BFE => 95% TYPE I
• BFE => 98% TYPE II
• 不同的BFE测试可以称为“修改版的Green&Vesley”或者体外BFE,这种方法在过去经常被使用。这种测试方法能提供较高的值,但并不真正的区分出不同质量外科口罩。这种体外BFE测试方法因此没有成为新的欧盟标准的一部分。
2. 呼吸阻抗 它是指气体在流经呼吸道及呼吸装置时的耗功加总值。
• 这种测试来确定口罩的气流阻力。
• 测试方法:使用一股定量的气流通过包含所有层的外科口罩样品。测量通过样品之前和之后的压力,这个不同的压力值再除以口罩的表面积(cm2)。
• 一个较低水平的呼吸阻抗值说明使用者使用起来更舒服。说明口罩戴起来感觉更加凉爽和更*呼吸,因为在材料上面的压力较小,所以口罩更*保持不变形。这样还能减少从口罩边缘呼出的未经过滤的气体。
分类
• 类别I&II(非防溅)= < 3.0 mmH2O/cm2
• 类别IR&IIR(防溅)= < 5.0 mmH2O/cm2
• 呼吸阻抗通常是用来测量每平方厘米材料上的值。一个增加舒适性的方法就是降低每平方厘米的呼吸阻抗,另外的一个方法就是通过增大口罩的表面积来增大口罩的可过滤的区域。
3. Splash Resistance (ASTM F1862-07)
防溅阻力 指防止血液\体液等溅撒 物的阻止能力.
• 这种测试是用来确定对潜在污染流飞溅的穿透阻碍作用。
• 测试方法:精确定量的人造血液在固定的压力下面通过样品口罩进行喷洒。常用的测试压力一般为80,120和160mmHg。可以通过观察样品口罩背面的是否有通过的液体的痕迹(红颜色)来判断。这个测试在每个压力条件下重复32次,3次以下的液体渗出,就可以判断产品在此压力下具有防溅性能。
• A higher splash resistance means the mask will protect the user in a better way against splashes of potentially contaminated fluid during a surgical procedure.
• 一个较高的防溅性能意味着这个口罩可以更好的保护在手术中使用者不受潜在的污染液体飞溅的侵害。
分类:
• 类别I和类别II不适用
• 类别IR和类别IIR至少为120mmHg
• 120 mmHg是个小的值。这个值和平均的收缩压相一致,用来防止由于小型动脉的破裂造成的小规模的血液飞溅。一些产品的保护级别甚至**过了120mmHg。
依据新的口罩的标准EN14683而定的的性能要求
欧盟标准分类 Bacterial Filtration Efficiency
过滤率 Breathing Resistance
呼吸阻抗
(mmH2O/cm2) Splash Resistance
防溅能力
(mmHg)
I 95% < 3.0 NA
IR 95% < 5.0 120
II 98% < 3.0 NA
IIR 98% < 5.0 120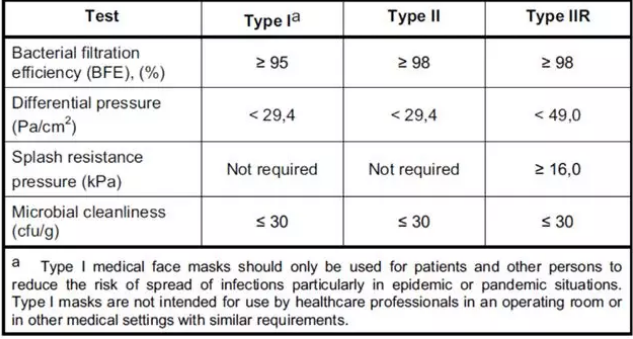
EN14683检测-EN14683含三部分检测:过滤率,呼吸阻抗,防溅阻力
我公司专业办理医疗产品出口欧盟、美国、中东南美等国家的各种认证:
TUV莱茵,TUV南德,***等CE认证(MDD/MDR法规),全套CE技术文件编订, CE*四版临床评价(MEDDEV 2.7.1 Rev 4)编写,欧盟授权代表,欧盟自由销售证书,ISO13485:二016,医疗器械单一审核程序(MDSAP)审核、美国FDA注册(含FDA510K申请),FDA美国代理人服务/ FDA QSR820验厂辅导及整改,FDA警告信应对&RED LIST REMOVAL/QSR820体系辅导/OTC验厂辅导及整改,英国BRC认证咨询,BSCI验厂辅导;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令辅导)。
EN14683含三部分检测:过滤率,呼吸阻抗,防溅阻力。
其中,过滤率就是常说的BFE检测,BFE/PFE/VFE是不同级别的过滤效果检测,PFE是比BFE级别更高的过滤效果检测,VFE是病毒过滤效果检测,检测实验室均为美国NELSON
检测项目(2014年新标准):BFE合并Different Pressure检测、合成血喷溅试验、微生物负载
SUNGO Technical Service Inc.在美国负责FDA美国FDA的业务运营。业务范围覆盖到所有的医疗器械产品、食品。提供的服务包括企业注册、产品列名、QSR820审厂辅导、审厂陪同、翻译、510K文件编撰、不符合整改、警告信应对、RED LIST移除等全项目的服务。
SUNGO Certification Company Limited在英国负责MHRA的业务的运营。SUNGO 英国公司按照欧盟相关指令、法规和指南的要求提供欧盟授权代表服务,协助境外制造商处理欧盟境内市场问题。同时获得MHRA授权开展MHRA产品注册和CFS,欧盟自由销售证的业务。截至目前,SUNGO已经为数百家客户提供了欧代服务,其中MHRA注册的客户近百家,CFS的客户增长也非常*。
SUNGO 中国致力于市场运营和客户服务,拥有行业内**的专业团队,同时与国际**认证机构例如TUV莱茵,SUD, ***, BSI, DNV,劳氏等机构保持良好合作关系。同时在国内医疗器械法规的合规服务中,提供*的辅导和技术支持。
SUNGO的*老师也是IECQ国际电工会标准制定组成员,参与电子电气行业国际标准制定。
SUNGO 专注于欧盟境外企业产品进口到欧盟、美国境内的符合性解决方案,特别是医疗器械、机电和环保领域的法规研究和应对,成功为**近千家企业提供了相关的技术服务和咨询,确保了其贸易的顺利开展。
欧盟个人防护口罩(非医疗器械)
欧盟个人防护口罩的欧洲标准是EN149,按照标准将口罩分为FFP1/FFP2/FFP3三个类别,需要满足欧盟(EU)2016/425个人防护设备指令(PPE)的要求。主流的防护口罩为FFP2/FFP3两类。
认证流程:
1. 产品的型式试验报告
2. 技术文件评审
3. 工厂质量体系审查
4. 颁发CE证书
5. 产品出口
注意:必须选择有PPE发证能力的发证机构申请,发证机构通过评审EN149报告后颁发CE-PPE证书。
NO.2
欧盟医用口罩(医疗器械)
医用口罩的欧洲标准是EN14683,按照标准将医用口罩分为TYPE Ia/TYPE II/TYPE IIR三个类别。Type Ia用于流行病期间的患者和其它人群,Type II和Type IIR用于医护人员。需要满足欧盟(EU)2017/745(新版医疗器械MDR)的要求。口罩在欧盟属于I类器械,但是分为I类非无菌和无菌两种。
1.非无菌口罩(现阶段只有这种可行)
1)编制技术文件
2)提供测试报告(例如熔喷布性能测试报告和无纺布的生物学报告)
3)提供符合性声明
4)*欧盟授权代表完成欧洲注册
时间估计:2-3个月
2.无菌口罩(现阶段新版MDR实施难度很大)
1)灭菌确认
2)ISO13485体系认证
3)编制技术文件
4)提供测试报告(生物学、性能、无菌等测试报告)
5)公告机构审核(目前几乎没有公告机构愿意接单)
6)获得CE证书
7)*欧盟授权代表完成欧洲注册
时间估计:1-2年,因此今年几乎是不可能了!
检测标准
1)生物学评价:ISO10993-1,-5,-10(常规三项)
2)过滤效率:EN 14683:2019附录B
3)呼吸阻抗:EN 14683:2019的附录C
4)防溅阻力:ISO 22609:2004
5)生物负载:EN ISO 11737-1:2018、EN 14683:2019附录D(同一批次检测数量不少于5个)
NO.3
美国FDA注册医用口罩
常见的医用口罩在美国FDA属于II类医疗器械,产品代码为FXX,规则号878.4040。除此之外还有OXZ口罩和OUK带/抗病毒介质的外科口罩。一般来说选择FXX类型的口罩。
510k申请流程:
1)进行产品测试(性能测试、生物学测试)
2)准备510k技术文件,提交FDA审评
3)获得FDA的510k批准信
4)完成工厂注册和器械列名
时间估计:6-10个月
注意:如已从途径获得N95认证并通过生物学、阻燃和血液穿透测试可豁免510k
口罩检测必须满足ASTM的标准,如下:
NO.4
美国NIOSH认证防护口罩
防护口罩需要获得NIOSH(美国国家职业安全卫生研究所)认证。按照过滤效率个人防护口罩可分成N95、N99、N100、R95、R99、R100、P95、P99、P100共9个类别。
按过滤网材质的过滤效率,可将口罩分为三种等级:N ,R ,P
N类的口罩只能过滤非油性颗粒物,比如:粉尘、酸雾、漆雾、微生物等。空气污染中的悬浮微粒,也多是非油性的。
R类的口罩只适合过滤油性颗粒物及非油性颗粒物,但用于油性颗粒物时限制使用时间不得**过8小时。
P类的口罩则既可过滤非油性颗粒物,又可过滤油性颗粒物。油性颗粒物比如:油烟、油雾等。
NIOSH认证系列口罩需符合42 CFR Part 84的要求,测试指标包括呼气阻力测试(Exhalation Resistance Test)、呼气阀泄漏测试(Exhalation Valve Leakage Test)、吸气阻力测试(Inhalation Resistance Test)、过滤效率测试(Sodium Chloride Test)等。
认证的申请需按照NIOSH的指南实施,企业需寄送样品至NIOSH实验室实施测试,同时提交技术性资料(包括质量体系资料)至NIOSH进行文件审核,只有文件审核和产品测试都通过,NIOSH才会核发认证。具体的认证则由NIOSH下属的NPPTL 实验室操作。
时间估计:2-3个月
今年2月1日,美国食品药品(FDA)医疗器械与放射健康中心(CDRH)生物制品评估与研究中心发布了《基于安全性和基本性能的途径》指南文件。该指南旨在描述一个基于安全性和基本性能的可选途径,使510(k)提交者只需验证新器械符合FDA既定性能标准,就可以证明新器械具有与合法上市器械相当的安全性和有效性。对该指南文件进行研究探讨,有助于我们借鉴国际先进经验和工作方式,提高我国医疗器械的审评效率,缩短审评时间,从而更好地促进我国医疗器械行业发展。
为了确定实质等同性,美国《联邦食品、药品和化妆品法案》*513(i)(1)(A)节规定,判定新器械具有与同品种医疗器械相同的预期用途,应符合如下要求:与同品种器械的技术特征相同;具有不同技术特征,与同品种器械具有实质等同性的资料,包含适当证明文件、经过认定的临床或科学数据,用于证明新器械具有与合法上市器械相当的安全性和有效性;与同品种器械相比,不会产生不同的安全性和有效性问题。
通过性能标准判定实质等同性
《基于安全性和基本性能的途径》指南(以下简称“指南文件”)的政策是扩展FDA长期以来通过简化510(k)程序应用进行医疗器械审批的方法。指南文件重点关注实质等同性分析的决**,要求510(k)提交者证明尽管存在技术差异,但新器械具有与合法上市器械相当的安全性和有效性。如果新器械满足合法上市器械在安全性和有效性方面相同特征的性能水平,FDA可以认定新器械具有与合法上市器械相当的安全性和有效性,同时支持基于表明新器械满足相应同品种器械性能水平的数据来核实实质等同性结果,而不是评审两种器械之间的直接测试数据对比。
根据指南文件中的方法,510(k)提交者可以仅证明新器械的性能符合既定性能标准,而这些性能标准可能描述在FDA指南、FDA认可共识标准和/或特殊控制文件中。通过证明新器械符合既定性能标准,提交者可以证明新器械具有与合法上市器械相当的安全性和有效性。
指南文件也提出,仅当FDA确定新器械符合以下情况时,方可使用既定性能标准:新器械适应证、技术特征不会产生与同品种器械不同的安全性和有效性问题;既定性能标准与新器械相同类型的合法上市器械的性能一致;新器械符合所有性能标准。如果新器械不能完全凭借FDA确定的既定性能标准来证明其提交材料的实质等同性,则不适合指南文件,但是,提交者仍可使用执行依据相应同品种器械进行直接性能比较的先前既定510(k)程序,包括传统、特殊和简化510(k)程序。
针对指南文件运行的工作计划
为保证指南文件顺利运行,FDA还将做以下准备:
预期用途和技术特征
FDA计划在既定性能标准中提供有关性能标准适用器械类型的信息,包括相关产品型号、适当的预期用途和适当的适应证。FDA还打算在其网站上维护适用基于安全性和基本性能途径的器械类型列表。如果对新器械是否符合FDA确定适用器械类型存有疑问,建议从相关办公室或部门寻求有关使用性能标准的适用性反馈。
确认性能标准
FDA计划在其网站为器械类型列表附上确认每种器械类型的性能标准的指南,以及指南文件中建议的测试方法(如可行)和其他相关信息。未在指南文件确定的性能标准,不得用于本程序。FDA依靠工作人员的经验和专业知识、文献资料以及对现有器械可用数据的分析,确定性能标准和相关测试方法,以支持实质等同性结果。
FDA评审数据
采用基于安全性、基本性能途径确定实质等同性的方法概述见附表。为了通过本程序获得实质等同性结果,通过提交符合FDA认可共识标准、测试方案、数据总结和/或基础数据(视情况而定)的声明,来证明新器械符合FDA认可的性能标准。必要时,FDA可以要求提交审评基础数据,证明新器械符合其既定性能标准和测试方法。
如果提供的数据不能证明新器械符合FDA确定的性能标准,将无法通过本程序确定实质等同性。提交者仍可以使用其他510(k)程序来证明实质等同性。
修改列表
FDA计划在网站上修订如前所述的器械类型列表,纳入附加器械类型,并根据指导规程(21 CFR 10.115)修订相应的性能标准和测试方法。FDA将定期评审适用标准和指南,修订或删除列表中的条目,特别是当性能标准不完全支持实质等同性决定时。从器械类型列表中删除之前,已通过基于安全性和基本性能途径获得的器械许可,将不会受到列表更改的影响