 7
7
刚结束的2月后两周,我们接到很多工厂关于医用口罩产品办理国内许可证书的申请。随着国内的口罩供应逐步缓解,同时海外的疫情发展加快,口罩产品出口需求已可以清晰预见。为应对近两天广大客户关于口罩出口认证的问询,SUNGO整理相关国家和地区法规要求以及我们可以提供的服务内容。摘要见表1
Part.1
欧洲市场
欧洲市场对于口罩的管理分为两个主要类别,个人防护口罩和医用口罩。个人防护口罩主要是工业用防护,医用口罩主要是医院使用。
医用口罩
医用口罩对应的欧洲标准是EN14683,该标准对于口罩的分类如下图所示,按照BFE、呼吸阻抗和防喷溅能力分为三个类别,具体指标见表2。
表2 欧洲医用外科口罩的分类
按照医疗器械法规2017/745/EU的要求,口罩产品可以按照一类器械进行管理。依据产品是无菌或非无菌状态提供,其认证模式不一样。
1.非无菌方式提供
1)编制技术文件
2)提供测试报告(可以提供熔喷布性能测试报告和无纺布的生物学报告)
3)编制DOC
4)*欧盟授权代表并完成欧洲注册
2.无菌方式提供
1)灭菌验证
2)建立ISO13485体系
3)编制技术文件
4)提供测试报告(口罩本身的生物学、性能、无菌等测试报告)
5)公告机构审核(目前只能按照MDR审核,预计近期没有NB可以审核)
6)获CE证书
7)*欧盟授权代表并完成欧洲注册
从目前整体情况来看,如果之前没有获得公告机构的CE证书,现在临时去申请已经没有可能性,因此目前出口到欧洲的口罩产品应该只有非无菌状态提供一个选项。但是非无菌并不是对生产环境完全不控制,EN14683对于产品的初始污染菌要求不大于30cfu/g。
2防护口罩
防护口罩的欧洲标准是EN149,按照标准将口罩分为FFP1/FFP2和FFP3三个类别,具体的指标见表3
。
表3 欧洲防护口罩分类
防护口罩需要满足欧盟个人防护设备指令(PPE)的要求,防护口罩属于其中复杂设计的产品。出口欧洲需要授权的公告机构进行认证并颁发证书,认证需要的资料包括:
A)产品的型式试验报告;
B)技术文件评审
C)工厂质量体系审查。
Part.2
美国市场
美国法规对医用口罩和工业防护口罩同样是区分管理,其中医用口罩由FDA管控,而防护口罩则由NIOSH管控。大家熟知的N95口罩就来源于NIOSH对口罩分类中的一个类别。
医用口罩
美国对于医用口罩的管理机构是FDA,在FDA系统中对于口罩的分类代码有如下3个。其中一个是外科口罩,一个是口罩,一个是带有/抗病毒介质的外科口罩,见图1。
三个类别的口罩都属于规则878.4040,分类都是II类,都需要申请510K批准。那么我们正常出口美国的口罩必须的路径为:
1)进行产品测试(性能测试、生物学测试)
2)准备510K文件,提交FDA评审
3)FDA发510K批准信
4)完成工厂注册和器械列名
5)产品出口
但是该过程至少需要半年以上时间。那是否有其他可选方法呢?SUNGO咨询师经过分析提供两种其他可选路径:
(1)已经获得NIOSH批准的N95口罩可以直接注册
从图2可以看出,如果你的N95口罩获得了NIOSH的批准,生物学测试、阻燃测试和血液穿透测试都通过了,那么你是可以豁免510K的,可以直接进行工厂注册和器械列名。
(2)获得持有510K的制造商的授权,作为其代工厂使用其510K批准号进行企业注册和器械列名。申请方需要获得授权书,需要签署正式的质量协议,FDA会进行核实和抽查。如果使用未经许可的号码,将会导致产品召回的风险。
2防护口罩
NIOSH将口罩分成N95、N99、N100、R95、R99、R100、P95、P99、P100合计9个类别。从某种意义上来说,N95算是其中防护级别比较低的品类。
NIOSH的口罩防护等级认证程序复杂,包括:
送样品到NIOSH认可的实验室进行预检,通常是美国实验室;
编写技术文件提交NIOSH评审,通常包括:
✰ 产品图纸
✰ 产品说明
✰ 质量体系文件
✰ 测试报告
工厂检查
核发证书
Part.3澳洲市场
澳洲的医用口罩按照I类管理,需要在TGA进行备案之后可以销售。当然在澳洲的备案需要由澳洲当地的SPONSOR来完成,其合规流程为:
1)*SPONSOR(SUNGO 澳洲可以提供服务)
2)完成技术文档
3)提交TGA进行备案
4)获得证书(见图3)
Part.4
加拿大
加拿大医疗器械产品分为4类,其中1类风险,不需要做器械注册(MDL),只需要进行MDEL(制造商注册),见图4。
图4 加拿大医疗器械管理示意图
加拿大的口罩产品属于I类医疗器械进行管控,按照其法规如果是中国制造商,可以选择:
1)申请MDEL证书自行出口
2)找到加拿大持有MDEL证书的进口商交易
申请MDEL需要完成申请表的如下内容,提交后2-4周可以获得证书。
(1)公司名称及联系方式
(2)许可文件、邮寄和帐单地址
(3)分类和活动表
(4)场地地址
(5)制造商信息
(6)证明
(7)签名
欧盟个人防护口罩(非医疗器械)
欧盟个人防护口罩的欧洲标准是EN149,按照标准将口罩分为FFP1/FFP2/FFP3三个类别,需要满足欧盟(EU)2016/425个人防护设备指令(PPE)的要求。主流的防护口罩为FFP2/FFP3两类。
认证流程:
1. 产品的型式试验报告
2. 技术文件评审
3. 工厂质量体系审查
4. 颁发CE证书
5. 产品出口
注意:必须选择有PPE发证能力的发证机构申请,发证机构通过评审EN149报告后颁发CE-PPE证书。
NO.2
欧盟医用口罩(医疗器械)
医用口罩的欧洲标准是EN14683,按照标准将医用口罩分为TYPE Ia/TYPE II/TYPE IIR三个类别。Type Ia用于流行病期间的患者和其它人群,Type II和Type IIR用于医护人员。需要满足欧盟(EU)2017/745(新版医疗器械MDR)的要求。口罩在欧盟属于I类器械,但是分为I类非无菌和无菌两种。
1.非无菌口罩(现阶段只有这种可行)
1)编制技术文件
2)提供测试报告(例如熔喷布性能测试报告和无纺布的生物学报告)
3)提供符合性声明
4)*欧盟授权代表完成欧洲注册
时间估计:2-3个月
2.无菌口罩(现阶段新版MDR实施难度很大)
1)灭菌确认
2)ISO13485体系认证
3)编制技术文件
4)提供测试报告(生物学、性能、无菌等测试报告)
5)公告机构审核(目前几乎没有公告机构愿意接单)
6)获得CE证书
7)*欧盟授权代表完成欧洲注册
时间估计:1-2年,因此今年几乎是不可能了!
检测标准
1)生物学评价:ISO10993-1,-5,-10(常规三项)
2)过滤效率:EN 14683:2019附录B
3)呼吸阻抗:EN 14683:2019的附录C
4)防溅阻力:ISO 22609:2004
5)生物负载:EN ISO 11737-1:2018、EN 14683:2019附录D(同一批次检测数量不少于5个)
NO.3
美国FDA注册医用口罩
常见的医用口罩在美国FDA属于II类医疗器械,产品代码为FXX,规则号878.4040。除此之外还有OXZ口罩和OUK带/抗病毒介质的外科口罩。一般来说选择FXX类型的口罩。
510k申请流程:
1)进行产品测试(性能测试、生物学测试)
2)准备510k技术文件,提交FDA审评
3)获得FDA的510k批准信
4)完成工厂注册和器械列名
时间估计:6-10个月
注意:如已从途径获得N95认证并通过生物学、阻燃和血液穿透测试可豁免510k
口罩检测必须满足ASTM的标准,如下:
NO.4
美国NIOSH认证防护口罩
防护口罩需要获得NIOSH(美国国家职业安全卫生研究所)认证。按照过滤效率个人防护口罩可分成N95、N99、N100、R95、R99、R100、P95、P99、P100共9个类别。
按过滤网材质的过滤效率,可将口罩分为三种等级:N ,R ,P
N类的口罩只能过滤非油性颗粒物,比如:粉尘、酸雾、漆雾、微生物等。空气污染中的悬浮微粒,也多是非油性的。
R类的口罩只适合过滤油性颗粒物及非油性颗粒物,但用于油性颗粒物时限制使用时间不得**过8小时。
P类的口罩则既可过滤非油性颗粒物,又可过滤油性颗粒物。油性颗粒物比如:油烟、油雾等。
NIOSH认证系列口罩需符合42 CFR Part 84的要求,测试指标包括呼气阻力测试(Exhalation Resistance Test)、呼气阀泄漏测试(Exhalation Valve Leakage Test)、吸气阻力测试(Inhalation Resistance Test)、过滤效率测试(Sodium Chloride Test)等。
认证的申请需按照NIOSH的指南实施,企业需寄送样品至NIOSH实验室实施测试,同时提交技术性资料(包括质量体系资料)至NIOSH进行文件审核,只有文件审核和产品测试都通过,NIOSH才会核发认证。具体的认证则由NIOSH下属的NPPTL 实验室操作。
时间估计:2-3个月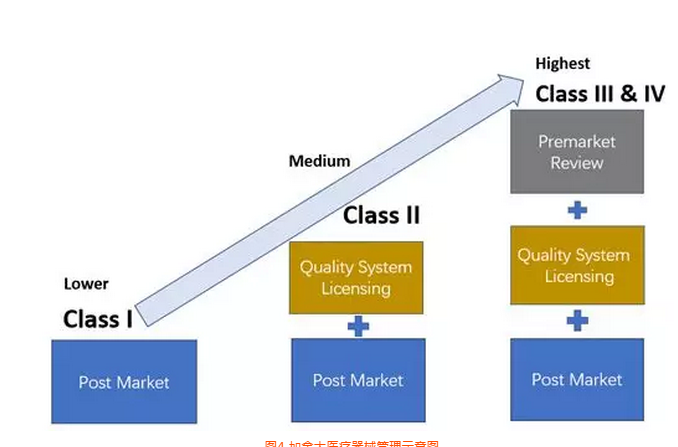
2019年12月10日,新的“ ISO 14971:2019医疗设备-风险管理在医疗设备中的应用”正式发布,过渡期三年。ISO 14971是医疗设备和体外诊断医疗设备风险管理的黄金标准。它初是为制造商提供的一种过程,可帮助其识别与设备相关的危害、健康风险以及如何有效地减轻它们。随着MDR和IVDR法规的陆续生效,各认证机构必将对风险管理相关文件的编制和更新提出新的要求。
PART
1
新版变化
新版标准相较于旧版,的变化是要求在风险管理计划中定义评估总体剩余风险的方法及其可接受性的准则。该方法包括收集和评审已上市的医疗器械或类似医疗器械的数据和文献。总体剩余风险的可接受性准则可以不同于单个风险的可接受性准则。除此之外,还有以下方面的变化:
12
标准结构框架采用了更高级别的十章架构,与其它管理体系标准保持了一致;
2
定义和术语的更新,比如利益、合理可预见的误用、现有的技术水平等;
3
强调了ISO 14971:2019的范围,可用于管理与医疗器械相关的风险,包括数据和系统安全相关的风险;
4
在对总体剩余风险进行评估和判断为可接受之后,将披露剩余风险的要求移动并合并到需求中;
5
医疗器械销售前合同的评审涉及到风险管理计划的执行。评审的结果记录到风险管理报告;
6
生产和生产后活动的要求已得到澄清和调整。更详细地说明了收集的信息,以及当收集的信息经过评审并确定与安全有关时应采取措施;
7
将2007版的附录C、附录D、附录F、附录G、附录H、附录J移到了ISO/TR 24971指南中,删减了附录I。
注:具体可见文末新旧版本对照表。
PART
2
MDR对风险管理的要求
除了以上新版的变化之外,欧盟医疗器械新法规对风险管理也提出了相关要求,包括:
01
为确保批量生产的器械继续符合MDR法规的要求,并且将生产的器械的使用经验纳入生产过程中,所有制造商均应具备质量管理体系和上市后监管体系,此类系统应与上述器械的风险级别和分类对应。此外,为尽可能降低器械相关的风险或防止与之相关事故的发生,制造商应建立风险管理体系,以及报告事故和现场安全纠正措施的系统。
02
风险管理体系应与器械的临床评估过程保持一致,并在该评估过程中反映,包括作为临床研究、 临床评估和上市后临床跟踪的一部分需解决的临床风险。风险管理和临床评估过程应相互依存,并应定期更新。
03
一般要求(附录 I,通用安全与性能要求)制造商应建立、实施、记录和维护风险管理体系。风险管理应理解为在器械整个生命周期中为连续迭代过程,需定期进行系统更新。进行风险管理制造商需做到:
(a) 制定并记录各器械的风险管理计划;
(b) 识别和分析与各器械相关的已知和可预见的危害;
(c) 估计和评价在预期使用时及在可合理预见的使用不当时产生的相关风险;
(d) 根据* 4 节的要求消除或控制(c)点所述的这些风险;
(e) 评估生产阶段,特别是上市后监管体系的信息、危害及其发生频率、评估其相关风险及总体风险、 风险利益比和风险可接受性。
(f) 根据(e)点所述信息影响的评估,必要时根据* 4 节的要求修改控制措施。
04
针对包含软件的器械或自身为器械的软件, 应根据现有技术开发和制造软件, 同时考虑开发生命周期原则、风险管理,包括信息安全、验证和确认。
05
器械带有一次性使用指示,在重复使用器械的情形下, 制造商已知的特性和技术因素相关信息可能会构成风险。此信息应基于制造商风险管理文档的特定部分,应详细说明这些特征和技术因素。
06
上市后监管计划应包括合适的指标和阈值,用于风险利益分析和风险管理连续的重新评估。
07
对于公告机构人员的要求,负责对产品进行相关审核人员应拥有风险管理及有关医疗器械标准和指导性文件方面的相应知识和经验。
08
对于制造商的产品验证人员的要求,具有合适资格和授权的人员的委任,以进行各个方面的检查,例如器械使用、生物相容性、临床评价、风险管理、杀菌等。
09
医疗器械临床前的风险管理评定,以及临床评价的流程相互作用。
10
公告机构应确保临床评价充分说明了GSPR规定的相关安全与性能要求。
11
制造商基于其对临床评价和风险管理的评估结果,判断 PMS 计划(包括 PMCF)是否充分。
12
高风险器械的风险管理中应包括风险利益分析与风险管理的总结,已知或可预见的风险相关的信息、任何不良反应、禁忌症和警告。应考虑到PMCF 评估报告的结论。
13
风险管理体系应与器械的性能评估过程保持一致,并在该评估过程中反映,包括作为性能研究、性能评估和上市后性能跟踪的一部分需解决的临床风险。风险管理和性能评估过程应相互依存,并应定期更新。
注:MD器械具体要求可参考ISO14971:2019Annex ZD;IVD器械可参考ISO14971:2019 Annex ZE。
我们可以看出,新版风险管理的标准更适用于MDR和IVDR法规,它强调了state of art和生命周期内实施风险分析、剩余风险及评估受益比的重要性。作为制造商会面临更加严峻的挑战,同时此标准为执行MDR、IVDR法规的符合性奠定了一定的基础。
EN14683检测,常用于防护服、手术衣、手套等产品的检测。它主要含三部分的检测:过滤率、呼吸阻抗、防溅阻力。其中过滤率就是常说的BFE检测,BFE/PFE/VFE是不同级别的过滤效果检测,PFE是比BFE级别更高的过滤效果检测,VFE是病毒过滤效果检测。
EN14683有EN14683:2005和EN14683:2014两种版本,其中2005版是旧版本,2014位新版本,现在做检测都是需要按照EN14683:2014标准来执行。