 8
8
通用规范
Reprocessing of Single-use Medical Devices
一次性医疗器械的再评审
Economic Operators
• 提出了新的概念Economic Operators经销链相关方,包括:制造商,欧盟授权代表,进口商和分销商
• 另新增加的要求:
• 各方都要明确其上游和下游的器械供应商;以及将器械直接供给的卫生机构或医疗保健专业人员(Article 25).
• Store and keep the UDI for implantable devices by economic operators (Article 27.8)
• Electronic system for registration of economic operators (Article 30+Annex VI, Part A)
Regulatory compliance
• It should be ensured that supervision and control of the manufacture of devices, and the post-market surveillance and vigilance activities concerning them, are carried out within the manufacturer’s organisation by a person responsible for regulatory compliance who fulfils minimum conditions of qualification.
• The authorised representative plays a pivotal role in ensuring the compliance of the devices produced by those manufacturers and in serving as their contact person established in the Union… legally liable for defective devices in the event that a manufacturer
established outside the Union has not complied with its general
obligations
我们可以为您提供的自主服务项目主要有:
出口欧洲法规:欧盟CE认证(CE整套技术文件编订、 CE*四版临床评价(MEDDEV 2.7.1 Rev 4)编写)、ISO13485:2016认证、欧盟授权代表(德国,英国和荷兰)、欧盟注册、欧盟自由销售证书、防护服PPE指令Type5/6认证
出口美国法规:医疗器械、化妆品、食品美国FDA注册(含FDA510K申请)、美国代理人、 FDA 验厂辅导及整改、FDA警告信应对&RED LIST REMOVAL、QSR820体系辅导、食品FDA验厂辅导及整改、OTC药品FDA验厂辅导及整改
中国法规:医疗器械产品备案登记表、医疗器械产品注册证、生产备案登记表、生产许可证、经营许可证、ISO9001/13485认证辅导、SFDA验厂辅导、SFDA注册检测、企业标准编制、药监局自由销售证。
出口其余国际法规:医疗器械单一体系审核MDSAP认证、澳大利亚TGA注册、BSCI验厂辅导、ISO22716 GMPC验厂辅导、BRC 认证,口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试
MDR分类规则的主要变化
• 仍为4类: Class I, IIa, IIb, III
• Duration of Use (无变化)
-Transient < 60 minutes;
- 60minutes < Short-term<30 days;
- Long term > 30 days
• 18 个规则=> 22个规则
- Rule 1-4 Non invasive devices
- Rule 5-8 Invasive devices
- Rule 9-12 Active devices
- Rule 13-22 Special rules
分类规则: 1-4 Non invasive devices
Rule 3:
• 在原来基础上, 新增由一种或几种物质混合组成的非侵入器械,其预期用于直接在体外接触已从人体或人体胚胎中取出且还未被植入人体的细胞、组织或器官,该类器械属于III类。
分类规则: 5-8 Invasive devices
Rule 6、 7:
• 在原来基础上, 新增专门用于直接接触心脏或循环系统的短暂、短期使用型侵入性手术器械属于III类
MDR分类规则的主要变化
分类规则: 5-8 Invasive devices
Rule 8:
• 在原来基础上,明确有源植入器械或其附件属于III类; 新增假体属于III类;关
节的全部或部分置换物(除钉、楔、板和工具等辅助组件外)属于III类;除钉、楔、
板和工具等组件外的植入性椎间盘置换物和接触脊柱的植入器械属于III类。
这部分的修订取代了现有的指令:
• 90/385/EEC Active implant medical device
• 2003/12/EC Breast implants raised to Class III
• 2005/50/EC Hip, knee and shoulder joint replacements raised to Class III
分类规则: 9-12 Active devices
Rule 9:
• 在原来基础上, 增加对发射电离辐射达到**目的的有源器械,以及控制、监控这些器械或直接影响这些器械性能的有源器械属于IIb类;
• 在原来基础上, 增加预期用于控制、监视或直接影响有源植入器械性能的有源器械属于III类
新增Rule 11:关于软件的分类规定,可以分为I, IIa, IIb,
III类:
• 提供用于作出诊断或**目的决策的信息的软件,属于IIa类,除非这些决定有可能影响:
- 死亡或个人健康状况不可逆转的恶化,属于III类;
- 个人的健康状况或外科手术严重恶化,属于IIb类。
• 用于监测生理过程属于IIa类,除非用于监测重要的生理参数,其中这些参数的变化可能导致对患者的即时危险,在这种情况下的软件属于IIb类。
• 其它属于I类
分类规则: 13-22 Special rules
Rule 16:
• 在原来基础上, 新增专门用于灭菌的器械属于IIa类,除非它们是专门用于消毒侵入性器械的消毒液或清洗消毒机,这种器械属于IIb类。
分类规则: 13-22 Special rules
Rule 18:
• 在原来基础上, 增加由人体的组织或细胞,或其无活性或使其无活性的物合成或制成的器械属于III类。
分类规则: 13-22 Special rules
新增Rule 19:由纳米材料合成或制成的器械的分类规则。
• All devices incorporating or consisting of nano material are classified as:
– class III if they present a high or medium potential for internal exposure;
– class IIb if they present a low potential for internal exposure; and
– class IIa if they present a negligible potential for internal exposure
分类规则: 13-22 Special rules
新增Rule 20:
• 除侵入性外科器械外,其他通过人体孔道吸入方式来用药的侵入性器械属于IIa类,除非它们的作用方式对用药的安全性和有效性有至关重要的影响或用于**危及生命的病症,在这种情况下属于IIb类。
我们可以为您提供的自主服务项目主要有:
出口欧洲法规:欧盟CE认证(CE整套技术文件编订、 CE*四版临床评价(MEDDEV 2.7.1 Rev 4)编写)、ISO13485:2016认证、欧盟授权代表(德国,英国和荷兰)、欧盟注册、欧盟自由销售证书、防护服PPE指令Type5/6认证
出口美国法规:医疗器械、化妆品、食品美国FDA注册(含FDA510K申请)、美国代理人、 FDA 验厂辅导及整改、FDA警告信应对&RED LIST REMOVAL、QSR820体系辅导、食品FDA验厂辅导及整改、OTC药品FDA验厂辅导及整改
中国法规:医疗器械产品备案登记表、医疗器械产品注册证、生产备案登记表、生产许可证、经营许可证、ISO9001/13485认证辅导、SFDA验厂辅导、SFDA注册检测、企业标准编制、药监局自由销售证。
出口其余国际法规:医疗器械单一体系审核MDSAP认证、澳大利亚TGA注册、BSCI验厂辅导、ISO22716 GMPC验厂辅导、BRC 认证,口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试
关于法规过渡期
MDR 过渡期为3 年,共涉及四个时间点(见表1):
欧盟医疗器械新法规MDR主要变化情况介绍
仅具有根据90/385/EEC 和93/42/EEC 指令签发的证书的器械可投放市场的前提是自MDR 适用之日起,其在设计和预期目的上无显著变化并符合新法规有关市场后监察、市场监察、警戒、经济运营商及器械注册的规定。
通过豁免指令的形式上市,且符合新法规的器械可在2020 年5 月26 日之前投放市场。并可在2020 年5 月26 日前*并通知符合新法规的符合性评估机构。公告机构可在2020 年5 月26 日前, 采用合规的符合性评估流程并按照新法规签发证书。
对于特定Ⅲ类器械和Ⅱ b 类器械产品,在已委派必要的医疗器械协调小组(MDCG)、*小组前提下,同样可通过指令豁免在2020 年5 月26 日之前投放市场。
法规关于公告机构的要求(正文*35~50 条) 自2019 年11 月26日起适用,即公告机构在新法规发布后的六个月内即应开始进行相应的申请,符合要求后方可依据新法规开展符合性评估。
同时法规对成员国主管机构的*和MDCG 的成立也设定了期限,要求于2019 年11 月26 日前完成。对于成员国主管机构之间的协调,设定期限为2019 年5 月26 日。
2016年12月14日,EUDAMED(European databank for medical devices) 筹划指导会上欧盟各国对于医疗器械法规MDR及IVDR的执行进行了一轮的讨论,与会人员对于这两个法规的细节内容进行了讨论并达成了一致意见。在此基础上,会议对于MDR及IVDR的执行达成了如下时间表。2016年12月14日,EUDAMED(European databank for medical devices) 筹划指导会上欧盟各国对于医疗器械法规MDR及IVDR的执行进行了一轮的讨论,与会人员对于这两个法规的细节内容进行了讨论并达成了一致意见。在此基础上,会议对于MDR及IVDR的执行达成了如下时间表。
主要事项 预计时间
英文版MDR及英文版IVDR定稿 2019年一月底
英文版MDR及IVDR在成员国发布
欧盟其他语言MDR 及IVDR在成员国发布 2019年2月中
欧盟会正式接受MDR及IVDR 2019年3月初
欧洲议会正式接受MDR及IVDR 2019年4月初
MDR及IVDR正式公开发布 2019年4月底
MDR及IVDR正式执行 2019年5月底
MDR强制执行 2020年5月底
IVDR强制执行 2022年5月底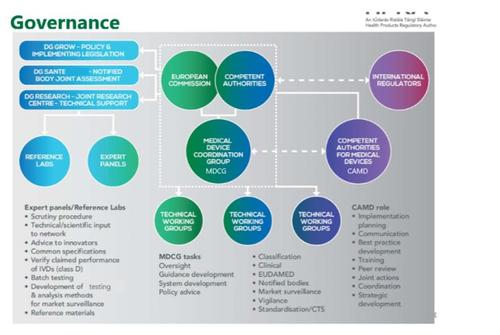
1、什么是临床评价
临床评估是一种持续收集,评估和分析有关医疗器械的临床数据的过程,通过对这些数据的评估及分析来确认是否有足够的临床证据来确认在依据制造商的说明书使用器械时,其安全和性能符合相关基本要求。临床评估是制造商的责任,其报告作为医疗器械技术文档的一部分。
2、为什么要进行临床评价
在医疗器械上市前,通过对其进行临床评价,(1)评估产品是否达到了预期目的;(2)在考虑预期性能的风险/获益时,已知的、可预见的风险和不良事件是否降到、并是可接受的水平;(3)所有安全有效的声明是否都有足够的证据支持。
当医疗器械上市后,需要通过建立的警戒系统和临床跟踪,对预期风险进行评估,以及**并发症,大规模使用下的安全及性能进行监测,并及时更新临床评估报告,为患者的生命健康提供**。
3、什么时候开始进行临床评价及临床评价更新要求?
临床评价是贯穿于医疗器械整个生命周期的一个持续的过程:
(1)临床评价在符合性评价阶段开展,将医疗器械的上市。
(2)随着在使用过程中有关该器械的新的临床安全性与性能信息的获得,对其进行周期性重复评估。
临床评价更新要求:
1.当制造商从PMS收到新的信息,有可能改变当前的评估;
2.如果没有收到新的信息:
(1)当器械带有重大风险或运行不好,则需每年更新一次;
(2)如果器械无明显风险且运行良好,需2-5年更新一次,但需要给出合理的理由。
4、怎样进行临床评价
临床评价是基于可利用的上市前和上市后临床数据的综合分析,包括临床性能数据和临床安全数据。
新版医疗器械临床评价指南MEDDEV 2.7/1 revision 4,将临床评价分为0-4个阶段,在临床评价过程中,阶段往往是反复的。事实上,鉴定和分析阶段可能会发现新的信息并提出新的问题,需要扩大评估范围,完善临床评估计划,并检索、评价和分析额定的数据。
欧盟医疗器械CE认证之——临床评价
阶段0:确定临床评估的范围及计划
临床评估开始之前,制造商应根据基本要求,需要从临床角度及器械历史及性质定义评估的范围及计划。
阶段1:相关数据的识别
用于临床评估的数据总的来说主要来自两个方面:制造商生成和持有的数据以及文献中的数据。其中,制造商生成和持有的数据包括:
(1)所有的上市前的临床研究;
(2)制造商在欧洲或其他国家进行的风险管理活动以及PMS项目;
(3)相关的临床前研究。
阶段2:相关数据的评估
为了确定阶段1获得的数据是否有价值,评估者应评估每一份文件对其临床性能和临床安全性的贡献。为了确保系统公正的评价数据,评估者在评估之前应当建立一个评估计划,用于确定评估过程和标准。
阶段3:临床数据分析
数据分析阶段的主要目标是确定当器械按其预期目的使用时,评估可供医疗器械使用的的数据集是否能证明符合器械临床性能和临床安全的基本要求。为证明符合性,评估者应从以下几个方面考虑:
(1)使用合理的方法;
(2)综合分析;
(3)考虑是否有增加临床研究及其他措施的必要;
(4)确定PMCF的需求。
阶段4:撰写临床评价报告 (可提供代理编写或更新:TUV南德/TUV莱茵/***/BSI/KIWA等公告机构要求的欧盟*四版医疗器械临床评价/评估报告、CE整套技术文件编订服务。)
对于所有的评价结果,将以报告的形式输出,即为临床评价报告。临床评价报告总结并汇总了所有相关的临床数据,并在技术文档的其他部分进行了记录或参考。
5、谁应该实施临床评价
临床评价应由合适的个人或团队进行。
制造商定义评价者的需求;
a)制造商应能够通过参考他们的资格和经验,来证明对评估者的选择,并为每一个评价者提出一个利益声明。
b)作为一般原则,评价者应具备以下知识:
●研究方法学(包括临床试验设计和生物统计学)
●信息管理(例如学科背景或图书馆员资格;相关数据库经验)
●法规需求
●医学写作(如有关科学或医学方面的研究生经验;有医学写作、系统复习和临床数据评估方面的培训和经验。
c)对于评估中的特定设备,评估者应该添加以下知识:
●器械的技术和应用
●诊断和管理的条件拟被设备、医疗替代品的知识、**标准和技术诊断或管理(例如相关医学专业的临床*)
d)评价者应该在相关领域具有以下培训和经验:
●在相关领域接受高等教育的学位和5年的专业经验;或
●如果没有相关学位,需要10年的专业经验。
2019 年4 月5 日,欧洲议会和理事会正式签发了欧盟关于医疗器械*2019/745 号法规(MDR,EU2019/745),5月5日,欧盟期刊(Official Journal of the EuropeanUnion) 正式发布该法规
2019 年5 月25 日,MDR 正式生效, 替代了原医疗器械指令(MDD,93/42/EEC)和主动植入式医疗器械指令(AIMD,90/385/EEC)。
MDR 由指令升级为法规,提高了对欧盟成员国的约束力,具有直接约束性,*各国转化为本国的法律法规的形式即可落实实施
MDR 在整合原指令的基础上,大幅提升了有关医疗器械认证的规范和限制,例如关于产品分类规则、器械的可追溯性、临床性能研究的规范、增加上市后的产品安全性和有效性的监管等方面。MDR 共10 章123 条,并附有17 个附录。
仅具有根据90/385/EEC 和93/42/EEC 指令签发的证书的器械可投放市场的前提是自MDR 适用之日起,其在设计和预期目的上无显著变化并符合新法规有关市场后监察、市场监察、警戒、经济运营商及器械注册的规定。
MDR 在很多方面的规定都趋于更加严格的监管模式,更加强调持续监管和*协作的监管方式。
医疗器械法规(MDR)转换期为3年,2020年5月4日起强制实行。体外诊断器械法规(IVDR)转换期为5年,2022年5月4日起强制实行。
MDR将有源医疗器械指令(现行的90/385/EEC)纳入了进来,与一般医疗器械指令(现行93/42/EEC)合二为一,IVDR直接取代了现行的体外诊断医疗器械指令98/79/EEC。
总的说来新的MDR和IVDR加强了体系管理,对高风险设备增加了相关规定比如对于非医疗用途但具有与医疗器械相似特性的设备也将受到新法规的管辖(如用于美容的彩色隐形眼镜),提升了产品对患者的透明度和可追溯性并设立电子数据库(Eudamed)、医疗设备将有一个的识别号这加强其在整个供应链的可追溯性。
法规对“医疗器械”的定义结合了90/385/EEC 和93/42/EEC 指令的范围,并有所扩大,纳入了有源植入医疗器械、软件以及植入或侵入人体的非医疗用途产品,如隐形眼镜、美容植入物、去除脂肪组织的器械、发射高强度电磁辐射进行皮肤**等操作的器械、利用磁场大脑神经元活动的器械等。对药械组合产品的描述也更为具体,法规还适用于使用活性或非活性动物、人源组织或细胞的产品制造而成的器械。
医疗器械的分类仍延续了之前的大类,即按照风险等级分为四大类:Ⅰ、Ⅱ a、Ⅱ b、Ⅲ类。但分类规则较之前有所增加,由18 条增加至22 条。具体分类规则条款情况及变化情况见下表2:
欧盟医疗器械新法规MDR主要变化情况介绍
我们可以为您提供的自主服务项目主要有:
出口欧洲法规:欧盟CE认证(CE整套技术文件编订、 CE*四版临床评价(MEDDEV 2.7.1 Rev 4)编写)、ISO13485:2016认证、欧盟授权代表(德国,英国和荷兰)、欧盟注册、欧盟自由销售证书、防护服PPE指令Type5/6认证
出口美国法规:医疗器械、化妆品、食品美国FDA注册(含FDA510K申请)、美国代理人、 FDA 验厂辅导及整改、FDA警告信应对&RED LIST REMOVAL、QSR820体系辅导、食品FDA验厂辅导及整改、OTC药品FDA验厂辅导及整改
中国法规:医疗器械产品备案登记表、医疗器械产品注册证、生产备案登记表、生产许可证、经营许可证、ISO9001/13485认证辅导、SFDA验厂辅导、SFDA注册检测、企业标准编制、药监局自由销售证。
出口其余国际法规:医疗器械单一体系审核MDSAP认证、澳大利亚TGA注册、BSCI验厂辅导、ISO22716 GMPC验厂辅导、BRC 认证,口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试
2019年5月5日欧盟发布OfficialJournal
在这里需要特别说明的是欧盟此次是直接发布的Regulation(法规)而相比较之前的Directive(指令)其区别在于:提高了文件的约束力,发布立即在欧盟成员国生效并成为有约束力的法律,此次的Regulation*向Directive那样需要经过成员国转化成当地法律法规去落实实施。
医疗器械法规(MDR)转换期为3年,2020年5月4日起强制实行。体外诊断器械法规(IVDR)转换期为5年,2022年5月4日起强制实行。MDR将有源医疗器械指令(现行的90/385/EEC)纳入了进来,与一般医疗器械指令(现行93/42/EEC)合二为一,IVDR直接取代了现行的体外诊断医疗器械指令98/79/EEC。
我们可以为您提供的自主服务项目主要有:
出口欧洲法规:欧盟CE认证(CE整套技术文件编订、 CE*四版临床评价(MEDDEV 2.7.1 Rev 4)编写)、ISO13485:2016认证、欧盟授权代表(德国,英国和荷兰)、欧盟注册、欧盟自由销售证书、防护服PPE指令Type5/6认证
出口美国法规:医疗器械、化妆品、食品美国FDA注册(含FDA510K申请)、美国代理人、 FDA 验厂辅导及整改、FDA警告信应对&RED LIST REMOVAL、QSR820体系辅导、食品FDA验厂辅导及整改、OTC药品FDA验厂辅导及整改
中国法规:医疗器械产品备案登记表、医疗器械产品注册证、生产备案登记表、生产许可证、经营许可证、ISO9001/13485认证辅导、SFDA验厂辅导、SFDA注册检测、企业标准编制、药监局自由销售证。
出口其余国际法规:医疗器械单一体系审核MDSAP认证、澳大利亚TGA注册、BSCI验厂辅导、ISO22716 GMPC验厂辅导、BRC 认证,口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试
其他
法规中规定了对于一次性使用器械的再处理即复用的要求。
MDR
*17 条规定,一次性使用的医疗器械的复用只能在相应国家法律允许的情况下进行,且应符合MDR 的规定。任何对一次性使用器械的再处理即复用的自然人或法人应视为复用器械的制造商,承担制造商义务,包括器械的可追溯性。但目前只有部分欧盟成员国接受器械复用并具备相应的法规规定。
MDR 在很多方面的规定都趋于更加严格的监管模式,更加强调持续监管和*协作的监管方式。如从监管层面自上而下确定了欧盟、各成员国、公告机构、经济运营商各自的义务和责任,同时从法规层面设定了成员国之间、公告机构之间及制造商与监管部门之间沟通和协作的制度及途径,从产品监管角度来讲,从产品生产质量体系建立和实施、符合性评估过程中的通用基本要求、技术文件建立、上市后监管文件建立、临床证据等上市前监管要求,到符合性评估程序要求,以及上市后监管、警戒和市场监管等措施,覆盖产品生命周期的全过程,并规定了信息管理的具体要求,包括UDI 及市场监管的电子系统等。
基于本版法规的医疗器械监管将很大程度上提高欧盟对医疗器械产品的要求,不论是制造商还是公告机构都将面临更严格的管理,基于目前的产品分类规则,更多的产品将需要执行公告机构参与的符合性评估流程,更多的品种纳入了医疗器械监管。