7
7
医疗器械MDD认证
医疗器械MDD认证
医疗器械CE认证简介
在医疗器械领域,欧盟会制定了三个欧盟指令,以替代原来各成员的认可体系,使有关这类产品投放市场的规定协调一致。分别为:
医疗器械指令MDD(Medical Devices):93/42/EEC,适用范围很广,包括除有源植入性和体外诊断器械之外的几乎所有的医疗器械。
体外诊断指令IVDD(In vitro diagnostic medical devices):98/79/EC,适用于血细胞计数器,妊娠检测装置等活体外诊断用医疗器械。
有源植入性医疗器械指令AIMDD(Active implantable medical devices):90/385/EEC,适用于心脏起搏器,可植入的泵等有源植入性医疗器械。
医疗器械MDD指令的分类等级
MDD指令根据不同的要求共分为6个等级,供认证机构评估:
等级 设计阶段 生产阶段
I类 自我符合声明 自我符合声明
I类(测量功能) 自我符合声明 申报机构
I类(灭菌) 自我符合声明 申报机构
II a类 自我符合声明 申报机构
II b类 申报机构 申报机构
III类 申报机构 申报机构
医疗器械CE认证所需技术资料
认证机构的统一评估包括根据指令规定的基本要求评审技术文件、根据标准EN 46001 或 EN/ISO 13485评审质量体系。医疗设备CE认证技术档案所需内容:
- 生产商/或欧洲代表名址;
- 产品及型号描述;
- EC符合声明书;
- 风险评估;
- 基本安全点检表;
- 适用之调合标准/或其他标准;
- 市场反馈及抱怨分析;
- 使用说明及标签;
- 授权代表;
- 线路、图表(适用的话);
- 计算书、测试报告或其它证明材料;
- 检验过程及过程描述;
- 灭菌或其它特殊过程(适用的话);
- 灭菌类产品的包装材料及方法;
-质量体系、质量手册;
I级医疗器械CE认证标记:
与其他类型的医疗设备相比,I类医疗设备被视为低风险设备。根据欧洲MDD,非无菌且不可测量的I类设备免于公告机构审核和认证。
牙科椅设备CE认证
1类医疗器械-示例
手臂、吊带、牙科椅、考试服、钳子、面具、病床可、重复使用的手术器械
夹板、灭菌包装、袜、de降压器
牙刷、尿袋、轮椅
1类设备可以分为三种,[a] 1类设备,[b] 1类无菌设备,[c] 1类测量设备:
[a] 1类设备
所有1类医疗设备都可以通过准备符合性声明并符合其他要求的自我声明来粘贴CE认证标志。但是大多数制造商仍然依赖第三方认证来获得的CE认证证书。
[b] I类无菌设备
等级1的无菌医疗器械CE认证标记,必须经过通知的身体参与。1级无菌制造商应执行ISO 13485并推荐认证,GMP控制是必要的。
[c] 1类测量设备
只有通过遵守MDD要求和协调标准,然后将技术文件提交*机构和现场审核,才能完成1类测量设备的CE认证标记过程。另外MEDDEV2。应遵循1/5指南。
怎么判断医疗设备-Class Im(测量设备)?
确定具有测量功能的设备的标准。
如果同时满足以下条件,则表明该设备具有测量功能:
1.该设备旨在定量地测量生理或解剖学参数,或者-测量能量或传递给人体或从人体去除的物质的数量或合格特性。
2.测量结果以法令80/181 / EEC的含义以法定单位或其他可接受的单位显示,或者与符合前述指令的法定单位或其他可接受的单位中指示的至少一个参考点进行比较。
3.预期目的隐含了明确或隐含要求的准确性。
本建议书不涵盖制造过程中的测量活动(包括用于校准目的的测量活动),并不表示制造的设备具有测量功能。
具有测量功能的I类设备的示例:
1.用于测量体温的非活动设备。
2.包括非活动温度显示的奶嘴。
3.用于指示体温**或低于*值的设备。
4.用于测量血压的非主动非侵入式设备。
5.用于测量眼压的非主动装置。
6.用于测量输送到人体或从人体排出的液体或气体的体积或流量的设备。
7.用于将液体输送到人体的设备(例如药勺,杯子,滴管,没有刻度或刻度)。
8.用于显示生理参数趋势的设备(例如没有刻度或刻度的尿液引流袋,肥胖卡尺)。
9.视力表
注:-假设相关的分类规则允许在类中分类,但前提是要满足相关的标准。
具有测量功能的1类设备在无菌条件下包装和提供,需要提供《合格机构证明》,而非无菌1类测量设备则不需要!
ISO 13485是自愿的
Ir类可重复使用的手术器械CE认证:
欧盟MDR 2017/745引入了可重复使用手术器械的新要求。所有可重复使用的手术器械均属于1r级,并需要经过认证机构的合格评定。
可重复使用的手术器械被定义为“在切割,钻孔,锯切,刮擦,刮擦,夹持,缩回,修剪或类似程序中用于外科手术的器械,未连接有源设备,制造商打算在使用后重新使用”已经执行了适当的程序,例如清洁,消毒和灭菌
外科手术器械CE认证
可以通过以下方法实现*20.1、20.3、20.4和20.5条以及*52条(7c)规定的MDR类Ir CE认证标记:
1.检验和测试每种产品或同类产品(附件IV)
2.根据附件VIII*1章*2.3节(附件V)和EN ISO 13485:2016审核生产质量保证体系(不包括设计)
3.终检验和测试审核(附件VI)EN ISO 13485:2016(不包括设计与制造)
4.全面质量保证体系审核(附件II)EN ISO 13485:2016
CE分类可能会因预期用途而异,请与MDD 93/42/EEC附件IX核对您的设备分类。
我们可以协助您:
1.医疗器械分类
2.确定MDR要求
3.确定统一标准
4.ISO 13485实施
5.识别公告机构
6.技术文件准备
7.技术文件提交给公告机构
8.重新提交技术文件
9.协助公告机构审核
10.协助解决不合格项
11.贴上CE认证标志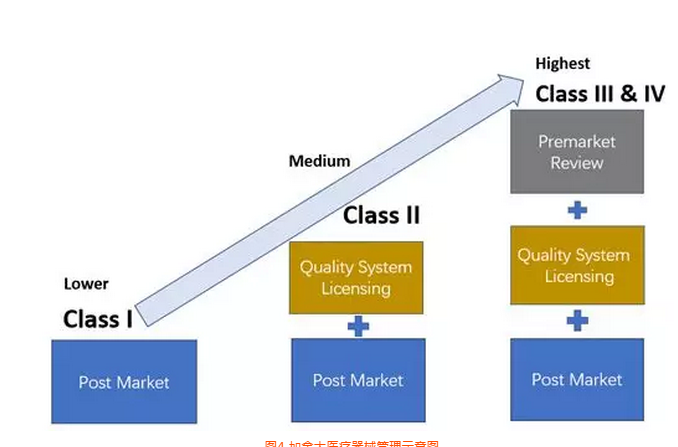
办理ce认证需要准备哪些资料,费用大概多少
CE的含义:
CE”标志是一种安全认证标志,被视为制造商打开并进入欧洲市场的护照。凡是贴有“CE”标志的产品就可在欧盟各成员国内销售,无须符合每个成员国的要求,从而实现了商品在欧盟成员国范围内的自由流通。 在欧盟市场“CE”标志属强制性认证标志,不论是欧盟内部企业生产的产品,还是其他国家生产的产品,要想在欧盟市场上自由流通,就必须加贴“CE”标志,以表明产品符合欧盟《技术协调与标准化新方法》指令的基本要求。这是欧盟法律对产品提出的一种强制性要求。
CE标志的意义在于:
用CE缩略词为符号表示加贴CE标志的产品符合有关欧洲指令规定的主要要求(Essential Requirements),并用以证实该产品已通过了相应的合格评定程序和/或制造商的合格声明,真正成为产品被允许进入欧共体市场销售的通行证。有关指令要求加贴CE标志的工业产品,没有CE标志的,不得上市销售,已加贴CE标志进入市场的产品,发现不符合安全要求的,要责令从市场收回,持续违反指令有关CE标志规定的,将被限制或禁止进入欧盟市场或退出市场。